遠(yuǎn)大醫(yī)藥(0512.HK)核藥抗腫瘤診療板塊再傳捷報(bào)����!
10月9日�����,遠(yuǎn)大醫(yī)藥發(fā)布公告稱��,公司全球創(chuàng)新溫度敏感性栓塞劑產(chǎn)品GPN00289在中國開展的用于原發(fā)性肝癌經(jīng)動(dòng)脈化療栓塞的注冊(cè)性臨床研究已于近日完成全部患者入組����。據(jù)悉����,GPN00289已獲得國家藥監(jiān)局創(chuàng)新型醫(yī)療器械資質(zhì)認(rèn)定����,該產(chǎn)品本次臨床進(jìn)展是遠(yuǎn)大醫(yī)藥在腫瘤介入方向上的又一次重大的研發(fā)進(jìn)展�,進(jìn)一步深化了公司在肝癌治療領(lǐng)域的布局���。
深化肝癌治療領(lǐng)域布局����,創(chuàng)新產(chǎn)品矩陣夯實(shí)全球競爭力
GLOBOCAN 2022年數(shù)據(jù)顯示,肝癌全球新發(fā)病例約87萬�,死亡病例約76萬�。我國國家癌癥中心2024年全國癌癥報(bào)告顯示����,2022年中國新發(fā)肝癌約37萬例(占全球42.5%)�����,死亡病例約32萬例(占全球42.1%)���。
手術(shù)切除是治療早期肝癌的方法����,但由于肝癌發(fā)病隱匿�����,早診困難,不足30%的肝癌患者在初診時(shí)適合根治性治療���,治療棘手,且預(yù)后較差��,發(fā)病率與死亡率之比高達(dá)1:(0.8-0.9)�����;即使通過根治性切除���,肝癌切除術(shù)后5年腫瘤復(fù)發(fā)轉(zhuǎn)移率高達(dá)50%~70%�,因此肝癌患者極需有效治療手段�����。
臨床上針對(duì)中晚期肝癌患者經(jīng)典的治療手段是經(jīng)導(dǎo)管動(dòng)脈化療栓塞術(shù)(TACE),目前常規(guī)TACE主要分為液體及固體栓塞�,固體栓塞效果較好,但是進(jìn)入末梢血管比較困難���;而液體栓塞雖然能栓塞末梢血管,但在體內(nèi)會(huì)被快速清除���,不能緩釋藥物,這些缺陷會(huì)影響TACE在肝癌治療中的效果�。
在此背景下���,遠(yuǎn)大醫(yī)藥GPN00289結(jié)合了液體栓塞和固體栓塞的優(yōu)勢,集載藥和栓塞為一體���,可彌補(bǔ)現(xiàn)有TACE治療手段的缺陷����,有望成為肝癌治療的更優(yōu)選擇����。
根據(jù)公告����,GPN00289具有溫度響應(yīng)且可塑高的特點(diǎn)�����,可隨溫度的變化發(fā)生液固相轉(zhuǎn)變�����,對(duì)大小不同��、形狀各異的血管都能進(jìn)行栓塞�����,且能有效防止側(cè)支循環(huán)的形成����,對(duì)動(dòng)脈血流的阻斷更完全�����、更持久有效,適用于各種富血管性實(shí)質(zhì)臟器腫瘤�,特別是肝臟富血管的良性及惡性腫瘤的栓塞治療。同時(shí)����,該產(chǎn)品還具有可降解特性��,可使得血管獲得多次治療機(jī)會(huì)����,并減少持久栓塞造成的不良反應(yīng),安全性高�,且可實(shí)時(shí)顯影�����,滿足手術(shù)精準(zhǔn)操作需求�。
值得注意的是��,GPN00289還具有載藥功能,除了可以與現(xiàn)有化療藥物進(jìn)行聯(lián)用外���,還有望與遠(yuǎn)大醫(yī)藥全球創(chuàng)新內(nèi)放射性治療藥物易甘泰®釔[90Y]微球注射液進(jìn)行聯(lián)用��,一方面��,可以進(jìn)一步提升產(chǎn)品對(duì)肝癌的治療效果���,另一方面,也有望進(jìn)一步拓展釔[90Y]微球注射液的潛在適應(yīng)癥。
公告還指出�,遠(yuǎn)大醫(yī)藥擁有GPN00289的全球權(quán)益,公司未來將積極推進(jìn)GPN00289的全球注冊(cè)開發(fā),致力于在中國及海外市場實(shí)現(xiàn)該產(chǎn)品與釔[90Y]微球注射液的戰(zhàn)略聯(lián)動(dòng),形成產(chǎn)品的協(xié)同效應(yīng)�����,持續(xù)深耕全球肝癌治療領(lǐng)域的科技創(chuàng)新�。
根據(jù)恒州博智的統(tǒng)計(jì)及預(yù)測��,2023年全球栓塞治療市場銷售額約為40.97億美元,預(yù)計(jì)2030年將達(dá)約65.36億美元��,年復(fù)合增長率約7.0%����。盡管市場空間較大���,但受限于研發(fā)技術(shù),目前布局栓塞劑的藥企較少,該領(lǐng)域仍是一片尚待開發(fā)的藍(lán)海市場��。遠(yuǎn)大醫(yī)藥憑借前瞻性的戰(zhàn)略布局����,已在該領(lǐng)域構(gòu)筑了創(chuàng)新產(chǎn)品矩陣并形成優(yōu)勢���,若未來公司GPN00289在國內(nèi)及海外市場順利獲批上市����,其全球市場潛力非?��?捎^���,有望進(jìn)一步推進(jìn)公司業(yè)績的提升�,并強(qiáng)化公司在肝癌治療領(lǐng)域的核心競爭力。
“Go Global”戰(zhàn)略鑄就全球核藥MNC,持續(xù)夯實(shí)企業(yè)地位
腫瘤介入是遠(yuǎn)大醫(yī)藥核藥抗腫瘤診療板塊中重點(diǎn)布局的戰(zhàn)略方向之一��,公司已在核藥抗腫瘤診療領(lǐng)域深耕多年��,已在該領(lǐng)域?qū)崿F(xiàn)研發(fā)、生產(chǎn)�����、配送�����、銷售等多個(gè)環(huán)節(jié)的多方位布局����,并以波士頓�����、成都為核心的研發(fā)基地����,波士頓�����、法蘭克福�����、新加坡���、成都所在的生產(chǎn)基地以及覆蓋全球50多個(gè)國家和地區(qū)的銷售網(wǎng)絡(luò)為基礎(chǔ)��,實(shí)現(xiàn)了全球化的核藥產(chǎn)業(yè)鏈布局��。
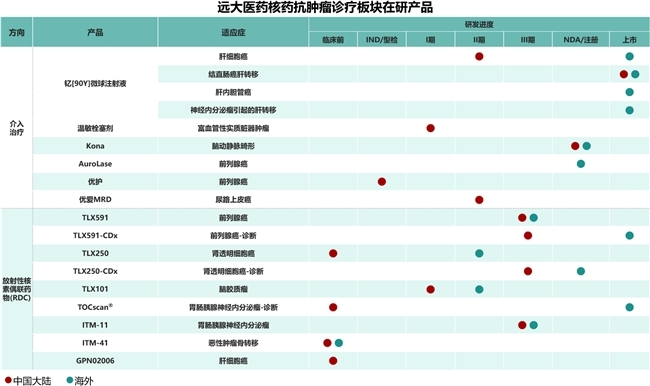
產(chǎn)品方面�����,遠(yuǎn)大醫(yī)藥圍繞腫瘤診療一體化的治療理念���,目前在研發(fā)注冊(cè)階段已儲(chǔ)備15款創(chuàng)新產(chǎn)品��,涵蓋68Ga、177Lu��、131I�、90Y、89Zr在內(nèi)的5種放射性核素�����,覆蓋了肝癌�、前列腺癌�����、腦癌等在內(nèi)的7個(gè)癌種��;早期研發(fā)階段以RDC藥物為主,產(chǎn)品儲(chǔ)備已達(dá)12款����。公司產(chǎn)品種類涵蓋診斷和治療兩類核素藥物�,為患者提供多適應(yīng)癥治療選擇�、多手段且診療一體化的抗腫瘤方案。
其中�����,釔[90Y]微球注射液于2025年7月在美國提前正式獲批新適應(yīng)證����,用于治療不可切除肝細(xì)胞癌(HCC)�����;于2025年9月獲歐洲CE標(biāo)志認(rèn)證新增多種肝癌適應(yīng)癥���,進(jìn)一步推動(dòng)該產(chǎn)品在不可切除肝癌治療領(lǐng)域的多方位覆蓋����,實(shí)現(xiàn)市場空間戰(zhàn)略級(jí)擴(kuò)容����。釔[90Y]微球注射液目前是獲美國FDA批準(zhǔn)用于不可切除HCC和結(jié)直腸癌肝轉(zhuǎn)移雙重適應(yīng)癥的選擇性內(nèi)放射治療產(chǎn)品�����,該產(chǎn)品在海外市場的順利推進(jìn),是遠(yuǎn)大醫(yī)藥“Go Global”戰(zhàn)略的階段性成果�����,不僅充分彰顯了遠(yuǎn)大醫(yī)藥優(yōu)秀的海外臨床注冊(cè)與商業(yè)化運(yùn)營能力�����,也為后續(xù)公司其他創(chuàng)新核藥產(chǎn)品的全球開發(fā)奠定了基礎(chǔ)。
研發(fā)方面���,遠(yuǎn)大醫(yī)藥正積極推進(jìn)創(chuàng)新核藥的全球臨床研究工作。2025年�,公司自研創(chuàng)新核藥GPN02006已取得突破性臨床進(jìn)展并斬獲國際會(huì)議的口頭報(bào)告,有望成為全球頭個(gè)針對(duì)GPC-3靶點(diǎn)的HCC診斷類RDC產(chǎn)品���。此外��,TLX591��、ITM-11等創(chuàng)新產(chǎn)品已加入國際多中心III期臨床試驗(yàn)����,充分彰顯公司在全球臨床研究的運(yùn)營實(shí)力����。
目前�����,遠(yuǎn)大醫(yī)藥是進(jìn)入中國III期臨床研究中診斷和治療類RDC創(chuàng)新藥總計(jì)儲(chǔ)備最多的企業(yè)����,也是全球范圍內(nèi)在核藥抗腫瘤領(lǐng)域擁有豐富產(chǎn)品管線和診療一體化布局的創(chuàng)新藥企之一。遠(yuǎn)大醫(yī)藥表示,公司未來將持續(xù)推進(jìn)核藥產(chǎn)業(yè)的全球化發(fā)展���,依托核藥平臺(tái)及產(chǎn)業(yè)鏈優(yōu)勢����,積極布局核藥創(chuàng)新產(chǎn)品,并堅(jiān)持自主研發(fā)創(chuàng)新核藥及“中美雙報(bào)”的策略�,持續(xù)推進(jìn)國際多中心臨床拓展全球市場����,促進(jìn)核藥產(chǎn)業(yè)以“Go Global”戰(zhàn)略高質(zhì)量發(fā)展�,打造核藥MNC�����。




評(píng)論